Reguloitujen alojen käännösvaatimukset: opas vaatimustenmukaisuuteen
- 4 päivää sitten
- 6 min käytetty lukemiseen

Reguloitujen alojen käännökset ovat paljon enemmän kuin kielellinen formaliteetti. Väärä sana lääkepakkauksen ohjeessa voi johtaa potilasturvallisuuden vaarantumiseen, viranomaissanktioon tai tuotteen vetämiseen markkinoilta. Pohjoismaisessa kielipilottikokeilussa on sallittu englanninkielinen pakkaus tietyissä sairaalalääkevalmisteissa, mutta suomen- ja ruotsinkielinen pakkausseloste on yhä pakollinen. Tämä käytännön esimerkki kertoo kaiken oleellisen: kielivaatimukset ovat dynaamisia, monikerroksisia ja äärimmäisen kriittisiä jokaiselle compliance-ammattilaiselle.
Sisällysluettelo
Tärkeimmät Huomiot
Kohta | Tiedot |
Käännösvaatimukset ovat tiukkoja | Säännellyillä aloilla käännösvaatimukset eivät ole muodollisuus vaan turvallisuuskysymys. |
Poikkeuksia on mutta harvoin | Pilotit mahdollistavat poikkeukset, mutta pääsääntö on kaksoiskielisyys etenkin Suomessa. |
Manuaalinen tarkistus on pakollista | Dokumenttien tulee käydä läpi sekä kääntäjän että tarkistajan läpikäynti ja dokumentoitu hyväksyntä. |
Laadukkaat kumppanit ehkäisevät virheitä | Kokeneet asiantuntijat ja järjestelmälliset prosessit tukevat vaatimustenmukaisuutta. |
AI voi tukea, mutta ei korvata ihmistä | Konekäännös toimii tukena, mutta ihmiskontrolli ja -vastuu ovat välttämättömiä reguloiduilla aloilla. |
Miksi käännösvaatimukset ovat ratkaisevia reguloiduilla aloilla
Reguloiduilla aloilla käännösvaatimukset eivät ole pelkkää byrokratiaa. Ne ovat suoraan kytköksissä turvallisuuteen, vastuukysymyksiin ja toiminnan lainmukaisuuteen. Yksi käännösvirhe voi muuttaa koko dokumentin merkityksen ja altistaa yrityksen mittaville seurauksille.
Lääketeollisuudessa käännösten turvallisuus on suoraan yhteydessä potilaiden hyvinvointiin. Jos lääkkeen annostusohjeen negaatio katoaa käännöksessä, potilas voi ottaa väärän annoksen. Vastaavasti rahoitusalalla virheellinen sopimusteksti voi johtaa taloudellisiin tappioihin tai oikeudenkäynteihin. Oikeudellisissa asiakirjoissa yksittäisen termin väärä käännös voi muuttaa sopimuksen koko tulkinnan.
Jokainen dokumenttityyppi kantaa oman vaatimustasonsa:
Lääkepakkaukset ja pakkausselosteet: kansalliset kielilait ja EU:n lääkelainsäädäntö
Kliiniset tutkimusraportit: ICH-ohjeet ja viranomaisten hyväksyntäprosessit
Rahoitussopimukset: kansalliset sopimuslait ja EU:n finanssilainsäädäntö
Tekninen turvallisuusdokumentaatio: EU:n koneasetus ja tuotevastuulainsäädäntö
Oikeudelliset asiakirjat: tuomioistuinten kielivaatimukset ja notariaattisertifiointi
Erityisen havainnollinen esimerkki on Fimean koordinoima pohjoismainen lääkepakkausten kielipilotin jatko, jossa kahden kielen vaatimus on pysynyt pakollisena Suomessa, mutta tietyissä erikoisvalmisteissa englanninkielinen ulkopakkaus on hyväksytty. Tämä osoittaa, että säännöt elävät ja compliance-ammattilaisen on seurattava muutoksia aktiivisesti.
“Pilotin laajentaminen ei tarkoita, että kielivaatimukset olisivat löystyneet, vaan että niiden soveltaminen on entistä tarkempaa ja tilannekohtaisempaa.”
Ammattilaisen vinkki: Älä oleta, että aiemmin hyväksytty käytäntö pätee enää tänään. Tarkista aina ajantasainen viranomaisohjeistus ennen uuden käännösprojektin aloittamista ja varmista, että säännösten mukainen käännösprosessi on dokumentoitu.
Keskeiset säädökset ja poikkeukset pohjoismaisilla markkinoilla
Pohjoismaisilla markkinoilla toimivien yritysten on navigoitava useamman kuin yhden maan lainsäädännössä samanaikaisesti. Vaikka pohjoismaat muodostavat yhteisen lääkepilotin, kansalliset vaatimukset poikkeavat toisistaan merkittävissä kohdissa.

Vuonna 2026 pohjoismaisessa pilotissa on 49 valmistetta, joissa englanninkielinen ulkopakkaus on hyväksytty, mutta suomen- ja ruotsinkielinen pakkausseloste on silti pakollinen. Tämä tarkoittaa, että ulkopakkaus voi olla englanninkielinen, mutta potilaan käsiin menevä seloste ei voi olla.
Maiden väliset erot käytännössä
Maa | Ulkopakkauksen kieli | Pakkausselosteen kieli | Pilottipoikkeus |
Suomi | Suomi ja ruotsi | Suomi ja ruotsi (pakollinen) | Englanti sallittu ulkopakkauksessa pienimenekkisille |
Ruotsi | Ruotsi | Ruotsi | Omat kansalliset käytännöt |
Tanska | Tanska | Tanska | Omat kansalliset käytännöt |
Norja | Norja | Norja | Omat kansalliset käytännöt |
Suomessa käännöstyypit säädellyissä toiminnoissa vaihtelevat sen mukaan, onko kyse kuluttajille suunnatusta tai ammattilaisille tarkoitetusta materiaalista. Sairaalalääkkeiden kohdalla pilotin mukainen englanninkielinen ulkopakkaus voi olla hyväksyttävä, koska käyttäjänä on terveydenhuollon ammattilainen, ei maallikko.
Vastuukysymykset ovat keskeisiä pilottipoikkeusten kohdalla:
Jos englanninkielinen pakkaus aiheuttaa väärinkäytöksen, vastuu on luovuttajalla
Poikkeuslupa ei poista valmistajan tuotevastuuta
Kielivaatimuksen lieventäminen sairaalaympäristössä perustuu ammattilaiskäyttöoletukseen
Dokumentaation on osoitettava, että poikkeuslupa on voimassa kyseiselle valmisteelle
Suuri uhka on niin sanottu vaatimustenmukaisuuden harha: yritys olettaa, että pilotin myöntämä poikkeus kattaa laajemman joukon valmisteita kuin se todellisuudessa kattaa. Tämä johtaa ongelmiin viranomaisauditoinneissa. Tarkka lääketieteellisten asiakirjojen käännös edellyttää aina tapauskohtaista arviota.
Tilastollinen huomio: Pohjoismaisessa pilotissa mukana olevien 49 valmisteen joukko on tiukasti rajattu. Suurin osa lääkepakkauksista ei kuulu pilotin piiriin, ja normaali kaksikielisyysvaatimus on edelleen voimassa niissä.
Teknisen dokumentaation käännösprosessin vaatimukset
Tekninen dokumentaatio on reguloiduilla aloilla erityisen herkkä alue. Pakkausseloste, kliininen tutkimusraportti, vaatimustenmukaisuusilmoitus tai koneen turvallisuusohje, jokaisella on oma prosessinsa ja erityisvaatimuksensa.
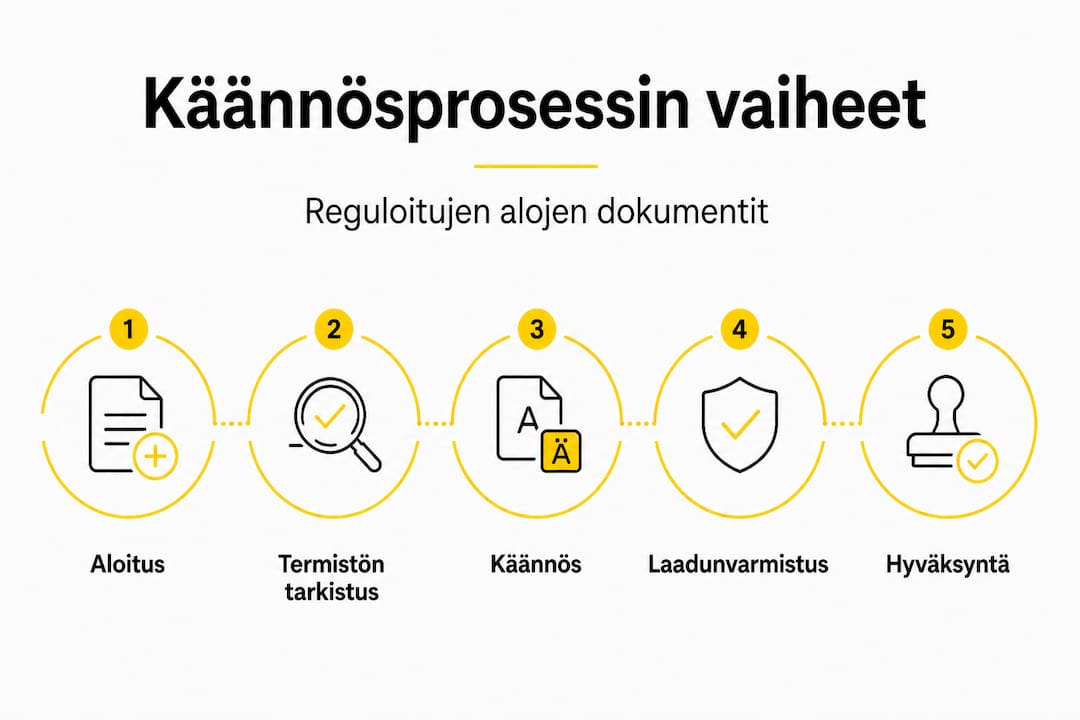
Teknisen dokumentaation käännösohjeet rakentuvat yleensä selkeän vaiheistuksen ympärille. Alla on kuvattu reguloidulle alalle sopiva käännösprosessi:
Dokumentin luokittelu ja vaatimusmäärittely. Ennen käännöstyön aloittamista on selvitettävä, mihin sääntelykehykseen dokumentti kuuluu. Onko kyse MDR:n alaisesta lääkinnällisen laitteen dokumentaatiosta, farmaseuttisen valmisteen pakkausselosteesta vai rahoitusteknisestä raportista? Jokaisella on oma vaatimustasonsa.
Termistöpankin ja käännösmuistin aktivointi. Ennen varsinaista käännöstä on integroitava olemassa olevat hyväksytyt termit ja aiemmat käännösmuistit. Tämä estää terminologian ristiriitaisuudet, jotka ovat yksi yleisimmistä virhelähteistä reguloiduissa käännösprojekteissa.
Alan asiantuntijan tekemä käännös. Pelkkä kielitaito ei riitä. Lääkinnällisen laitteen dokumentaation kääntää henkilö, jolla on lääketieteellinen tai biotekninen tausta. Juridisen sopimuksen kääntää juristikoulutuksen saanut kielentaitaja.
Riippumaton tarkistus. Kääntäjä ja tarkistaja ovat eri henkilöt. Tarkistaja vahvistaa sekä kielellisen että sisällöllisen oikeellisuuden viranomaisvaatimusten valossa. Tämä kaksoisvarmistus on ISO 17100 -standardin vaatimus.
Validointi ja hyväksyntä. Käännetty dokumentti käy läpi virallisen hyväksyntäprosessin, johon voi kuulua sekä asiakkaan sisäinen hyväksyntä että tarvittaessa viranomaistarkistus.
Arkistointi ja jäljitettävyys. Kaikki käännösversiot, muutoshistoria ja hyväksyntämerkinnät tallennetaan järjestelmällisesti. Tämä on edellytys viranomaisauditoinnille.
Pakkausselosteiden kielivaatimuksia on pilotin puitteissa lievitetty tietyiltä osin, mutta laatu ja tarkkuusvaatimukset pysyvät muuttumattomina. Tämä tarkoittaa, että prosessin tiukkuus ei vähene, vaikka kielivalikoima joustaisi.
Dokumenttityypin vaikutus käännösprosessiin
Dokumenttityyppi | Erityisvaatimus | Tarkistustaso | Sertifiointi |
Lääkepakkauksen seloste | Kaksikielisyys (FI/SV) | Kaksoisvalidointi | MDR, Fimea |
Kliininen tutkimusraportti | ICH E3, tieteellinen tarkkuus | SME-tarkistus | GCP-sertifioitu kääntäjä |
Rahoitussopimus | Oikeudellinen tarkkuus | Juristin tarkistus | Notariaatti tarvittaessa |
Tekninen turvallisuusohje | Koneasetus, tuotevastuu | Insinööritarkistus | CE-prosessin mukainen |
Patenttiasiakirja | Tekninen ja juridinen | Kaksois-SME | EPO:n vaatimukset |
Ammattilaisen vinkki: Tietoturva ei ole valinnainen ominaisuus käännösprosessissa. Patenttihakemukset, kliiniset tutkimustiedot ja sopimukset sisältävät immateriaalioikeudellisesti suojattua tietoa. Julkisten käännöstyökalujen, kuten DeepL:n tai Google Translaten, käyttö tällaisissa projekteissa rikkoo GDPR:ää ja NDA-sopimuksia, koska data siirtyy palveluntarjoajan palvelimille. Laatuvaatimukset säädellyille aloille edellyttävät suljettua tietoympäristöä.
Laadunvarmistus ja riskienhallinta käännösprojekteissa
Käännösprosessin tekninen tarkkuus on vain osa kokonaisuudesta. Systemaattinen laadunvarmistus ja riskienhallinta ratkaisevat sen, pysyykö projekti viranomaishyväksynnässä ja välttyykö yritys kalliilta korjaukselta.
Tietoturvalliset käännökset ovat perusedellytys, mutta laadunvarmistus menee syvemmälle. Se tarkoittaa dokumentoitua prosessia, jossa jokainen vaihe on jäljitettävissä ja vastuutettu.
Keskeisiä laadunvarmistuksen elementtejä reguloiduissa käännösprojekteissa ovat:
Kaksoisroolien erottelu. Kääntäjä ja tarkistaja eivät voi olla sama henkilö. ISO 17100 edellyttää tätä erottelua, ja se on käytännössä tärkein yksittäinen tae virheenkorjaukselle.
Terminologian hallinta. Hyväksytty termipankki on päivitettävä aina, kun lainsäädäntö tai viranomaisohjeet muuttuvat. Vanha termi vanhassa käännösmuistissa on piilevä riski.
Muutostenhallinta. Kun lähdeteksti päivittyy, käännettyjen versioiden päivitys on tehtävä systemaattisesti. Käytännössä tämä tarkoittaa versionhallintajärjestelmää, joka tunnistaa muutokset automaattisesti.
Jäljitettävyys ja auditointiketju. Jokaisesta käännösprojektista on oltava tallennettu: kuka käänsi, kuka tarkisti, milloin, mitä versioita käytettiin ja miten hyväksyntä dokumentoitiin.
Viranomaiskommenttien hallinta. Kun viranomainen pyytää muutoksia, kaikki korjaukset on kirjattava ja päivitettävä yhtenäisesti kaikkiin kieliversioihin.
Yleisimmät riskipisteet reguloiduissa käännösprojekteissa ovat:
Epäjohdonmukainen terminologia eri dokumenttien välillä
Päivitetyn lähdetekstin osittainen käännättäminen
Tarkistusvaiheen ohittaminen aikataulupaineen alla
Tietoturvan laiminlyönti julkisia käännöstyökaluja käytettäessä
Poikkeuslupien soveltaminen liian laajaan dokumenttijoukkoon
Suomessa laatu on viranomaisvaatimus, ei lisäpalvelu. Pilotin puitteissakin suomen- ja ruotsinkieliset pakkausselosteet ovat pakollisia, mikä osoittaa, että laadun dokumentointi pysyy keskiössä kaikissa olosuhteissa.
Riskienhallinta alkaa jo projektin suunnitteluvaiheessa. Käännösvirheiden välttäminen edellyttää, että compliance-ammattilainen osallistuu projektin määrittelyvaiheeseen, ei pelkästään lopputuloksen tarkistamiseen. Mitä myöhemmässä vaiheessa virhe löydetään, sitä kalliimpaa sen korjaaminen on.
Ammattilaisen vinkki: Rakenna käännösprojektiin aina erillinen laadunvarmistustarkistuslista, joka perustuu kyseisen dokumenttityypin viranomaisvaatimuksiin. Generinen tarkistuslista ei riitä, kun kyse on MDR-dokumentaatiosta tai EBA:n vaatimustenmukaisuusraporteista.
Usein unohtuva näkökulma: miksi sääntely ei riitä ilman kokeneita käännöskumppaneita
Tässä on ajatus, jota harvoin sanotaan ääneen: lainsäädäntö antaa kehykset, mutta se ei ratkaise ongelmaa. Compliance-ammattilaiset tietävät tämän omasta kokemuksestaan. Viranomaisohje kertoo, mitä pitää tehdä, mutta ei, miten se tehdään oikein käytännössä.
Pohjoismaisessa lääkepilotissa tämä konkretisoituu selkeästi. Viranomainen myöntää jouston englanninkieliseen ulkopakkaukseen, mutta pakkausselosteen kielivaatimus pysyy. Moni yritys kompastuu juuri tähän kohtaan: pilotin logiikka ymmärretään vain osittain, ja soveltaminen menee vikaan. Kokenut käännöskumppani, jolla on syvä ala- ja viranomaisosaaminen, tunnistaa tämän sudenkuopan etukäteen.
Erikoistuneet käännöskumppanit tuovat mukanaan kolme asiaa, joita sääntely yksin ei voi tarjota. Ensimmäinen on jatkuva sääntelymuutosten seuranta. Regulaatio elää, ja 2026 voimaan astuneet muutokset voivat tehdä vuonna 2024 hyväksytyistä prosesseista vanhentuneita. Toinen on alan termistön hallinta, joka ylittää kielitaidon ja edellyttää substanssiosaamista. Kolmas on prosessikehitys: systemaattinen, auditoitava käännösprosessi, joka kestää viranomaistarkastuksen.
Vakiintunut yhteistyö käännöskumppanin kanssa tuottaa myös mitattavia liiketoimintahyötyjä. Käännösmuistit karttuvat, ja aiemmin käännetyt hyväksytyt kappaleet voidaan hyödyntää uudelleen. Tämä nopeuttaa prosessia merkittävästi ja vähentää virheiden todennäköisyyttä, koska aiemmin validoitua sisältöä ei käännetä uudelleen tyhjästä. Pitkäaikainen kumppani myös oppii yrityksen erityistermistön ja toimintaympäristön, mikä parantaa käännösten johdonmukaisuutta koko dokumentaatioketjussa.
On myös rehellisesti sanottava, että teknologia on muuttanut kentän pysyvästi. Julkiset tekoälytyökalut ovat tehokkaat, mutta täysin sopimattomia reguloidulle alalle. Niiden käyttö kliinisten tutkimustietojen tai patenttihakemusten kääntämiseen on tietosuojarikkomus. Suljettu, EU-palvelimilla toimiva LLM-pohjainen AI yhdistettynä alan asiantuntijakääntäjien AI+HUMAN-prosessiin on ainoa tapa yhdistää nopeus, tarkkuus ja tietoturva.
Tässä on mielestämme alan suurin väärinkäsitys: monet yritykset etsivät halvinta tai nopeinta ratkaisua, kun heidän pitäisi etsiä luotettavinta. Reguloiduilla aloilla virhe ei näy vain projektin laskussa, vaan viranomaissanktioissa, tuotevetoina tai oikeudenkäyntikuluina.
Tee työstäsi helpompaa vaatimustenmukaisten käännösten avulla
Vaatimustenmukaisuuden varmistaminen reguloiduilla aloilla vaatii enemmän kuin hyvän prosessin. Se vaatii kumppanin, joka ymmärtää sekä alan lainsäädännön että sen käytännön soveltamisen. AD VERBUM on toiminut yli 25 vuotta juuri tässä risteyksessä, lääketieteen, oikeuden ja rahoituksen vaativimmissa käännösprojekteissa.
AD VERBUM:n AI+HUMAN -malli yhdistää suljetun, ISO 27001 -sertifioidun LLM-pohjaisen tekoälyn yli 3 500 alan asiantuntijakääntäjän osaamiseen. Tämä tarkoittaa, että arkaluonteiset dokumentit eivät koskaan poistu EU-palvelimiltamme, ja jokainen käännös tarkistetaan substanssiasiantuntijan toimesta. Käytännössä saat kolme kertaa nopeamman toimituksen ilman tietoturvariskin kasvua.
Tutustu Life Sciences -ratkaisuihin tai katso, miten asiantuntevat käännöspalvelut sopivat teidän compliance-prosessiinne. Asiantuntijamme auttaa löytämään oikean toimintamallin jo ensimmäisessä keskustelussa.
Usein kysytyt kysymykset
Milloin englanninkielinen pakkaus on sallittu lääkkeissä Suomessa?
Englanninkielinen pakkaus on sallittu vain pohjoismaisessa pilotissa pienimenekkisille sairaalalääkkeille, ja tällöinkin vaaditaan suomen- ja ruotsinkielinen pakkausseloste.
Tarvitseeko kaikki säädelty dokumentaatio käännettä aina kahdelle kielelle Suomessa?
Yleensä kyllä, esimerkiksi lääkealan pakkauksissa suomen- ja ruotsinkielisyys on lähes aina pakollista, ja pilotin poikkeukset koskevat vain tiukasti rajattua valmistejoukkoa.
Miten varmistetaan, että käännösprojekti täyttää kaikki viranomaisvaatimukset?
Systemaattinen käännös- ja tarkistusprosessi sekä laadun dokumentointi takaavat vaatimustenmukaisuuden, sillä jäljitettävyys on viranomaisauditoinnin perusedellytys.
Mitkä ovat yleisimmät käännösprojektin riskipisteet reguloiduilla aloilla?
Merkittävimmät riskit liittyvät terminologian epäjohdonmukaisuuteen, päivitysten osittaiseen käännättämiseen ja tarkistusvaiheen ohittamiseen aikataulupaineen alla.
Voiko AI-käännöksiä käyttää säädellyn alan dokumentaatiossa?
AI-käännöksiä voi käyttää tukena suljetussa, tietoturvallisessa ympäristössä, mutta julkisten työkalujen käyttö rikkoo tietosuojavaatimuksia, ja ihmisen tekemä asiantuntijatarkistus on aina välttämätöntä.
Suositus